TERMOMETROS DE DILATACIÓN
Termómetros de líquido en vidrio
El vidrio del termómetro debe elegirse por su estabilidad y debe estar bien recocido. El bulbo, a altas temperaturas y presiones, está expuesto a aumento permanente de volumen, ocasionando que la indicación del termómetro sea más baja de lo debido.
Los termómetros de mercurio más exactos están graduados y calibrados para inmersión total; esto es, con todo el mercurio, incluyendo el del tubo, a la temperatura que se está: midiendo. Si parte del mercurio de la columna se extiende fuera de la región en que se ha de medir la temperatura, hay que aplicar una corrección a la lectura, basada en la longitud en grados de la columna emergente, en la diferencia de temperatura entre la columna emergente y el bulbo y en la ditalación relativa del mercurio y del vidrio.
Termómetro de Beckmann
El termómetro diferencial de Beckmann tiene una escala de 30 cm de largo, aproximadariiente, con una escala total de 5 6 6 grados C. en divisiones. de 0.01 de grado. Está construido de suerte que una parte del mercurio del bulbo puede ser trasladada a un depósito de manera que lleve el extremo de la columna de mercurio a la sección graduada para las zonas de temperaturas en que se han de medir las diferencias. Se emplea sólo para medir diferencias cle temperatura. La exactitud conseguida está entre 0.002 y 0.005 grados en la medida de cualquier intervalo dentro de los límites de la escala.
Termómetro de cinta bimetálica
Este termómetro consiste en una cinta hecha de dos metales de coeficientes de dilatación térmica muy diferente, tales como el Invar y el latón, soldados cara con cara en toda su longitud. La cinta puede ser casi recta o puede formar una espiral para conseguir mayor sensibilidad. Una elevación de temperatura cambia la curvatura de la cinta, puesto que el latón aumenta más rápidamente en longitud que el Invar. Si uno de los extremos es fijo, un indicador unido al extremo libre se mueve sobre una escala graduada en temperaturas o una pluma se mueve sobre una tarjeta movible para registrar la temperatura. Las cintas bimetálicas se emplean para obrar sobre contactos eléctricos que controlan la temperatura de habitaciones, baiíos de aire y hemos. Dentro del intervalo.
La respuesta a los cambios de temperatura es casi lineal. Dentro del intervalo de temperaturas aceptado (no superior a 1500 C. cuando se emplea el latón, considerablemente superior cuando se emplea en lugar del latón una aleación de cromo y níquel), los errores inherentes a la cinta son insignificantes. Pueden ocasionarse errores apreciables en el enlace mecánico. Hay una frna , la cual la cinta bimetálica es una espiral dentro de un tubo delgado de metal, y la aguja indicadora se mueve sobre una escala circular graduada, coaxial con el tubo. Puede reemplazar al termómetro de mercurio para numerosos usos.
Termómetros de sistemas llenos
Termómetros llenos de gas
El termómetro de gas de volumen constante, mencionado al hablar del establecimiento de la escala termodinámica de temperaturas, pertenece a la categoría de tennómetros llenos de gas y es el más exacto de este tipo. Sólo se emplea en los laboratorios de patrones a causa de su complejidad y de su tamaño. Para usos industriales, un termómetro por presión de gas consta de un elemento que mide la presión, como el tubo Bourdon conectado por un tubo capilar a una ampolla que se expone a la temperatura que se ha de medir. El sistema se llena, a presión, con un gas inerte, ordinariamente el nitrógeno. Puesto que la presión del gas en un recipiente cerrado es proporcional a su temperatura absoluta, el elemento medidor puede ser calibrado en grados de temperatura con una escala dividida uniformemente. Como el gas del elemento medidor y del tubo de conexión no está a la temperatura del bulbo, el volumen de éste tiene que ser grande para que los errores introducidos por la diferencia de temperatura del elemento medidor de la presión y del tubo capilar resulten insignificantes. El bulbo debe tener por lo menos cuarenta veces el volumen del resto del sistema. Por ello, y a causa del retardo en la transmisión de los cambios de presión por el tubo capilar, la longitud de éste se limita a un máximo de 60 m, y es preferible mucho menos.
La presión inicial en el termómetro de gas es ordinariamente de 10 a 35 Kg/cm². El par de torsión producido es entonces amplio para operar una pluma registradora cuando la dimensión de la escala es 200 grados centesirnales, o más. Las dimensiones de la escala menores de 50 grados no son recomendadas. Con una dimensión de escala de 200 grados, o más, la reproducibilidad de las lecturas es del orden de +- 1/4 % de aquella dimensión. El tiempo de respuesta tiende a ser largo, en parte a causa de la necesidad de transmitir los cambios de presión por medio de un tubo de calibre fino y en parte a causa del gran volumen y escasa conductividad térmica del nitrógeno. Para el volumen suficiente, el bulbo tiene ordinariamente 22 mm de diámetro, lo que da una respuesta lenta. El tiempo de respuesta puede ser disminuido consiguiendo el volumen deseado mediante el empleo de un tubo largo de 6.5 mm, ordinariamente en forma de hélice de 5 cm.
La temperatura es indicada por una aguja que se mueve sobre una escala graduada o se registra en un papel de gráficas sobre un cilindro por una pluma accionada por el elemento que mide la presión. La escala para los registradores rara vez es menor de 100 grados centesimales, pero en los aparatos indicadores el campo puede ser menor.
Las variaciones en la presión barométrica no suelen ser tan grandes que afecten apreciablemente las indicaciones pero los grandes cambios en altitud deben ser corregidos en la graduación.
Los termómetros de gas a presión se emplean en temperaturas entre -450 °F. y + 1000 °F. (-268 °C. y + 538 °C.), lo cual queda parcial o enteramente fuera de los límites de los sistemas de vapor a presión y en aplicaciones en que la menor exactitud y el mayor tamaño del bulbo no exigen la elección de un termómetro de alto costo del tipo de expansión de líquido.
Termómetros de vapor a presión
Los termómetros de vapor a presión utilizan el hecho de que en una vasija cerrada que no contiene más que un líquido y su vapor, llenando el líquido sólo parcialmente, el recinto, la presión es dependiente solamente de la especie del líquido y de su temperatura. Un uso muy extenso se hace de esta relación entre la presión del vapor y la temperatura en la medida y registro de las temperaturas industriales.
El termómetro de presión de vapor (fig. 1) se parece al termómetro de gas a presión en que consta de un bulbo, un tubo de conexión de longitud fija, de 1.5 a 75 m de largo, y un elemento sensible a la presión (fig. 2).
Termómetro de vapor a presión Elemento sensible a la presión
El bulbo está parcialmente ocupado por un líquido con una temperatura de ebullición bastante baja para producir una presión de trabajo de 5 a 35 Kg/cm² en el intervalo de temperaturas a cubrir. El extremo superior de este intervalo debe ser mas bajo que el punto crítico del líquido. Se emplean el cloruro de metilo, el anhídrido sulfuroso, el éter, el alcohol etílico y el tolueno, elegidos para la presión de vapor apropiacla según las relaciones de temperatura, la inercia de los metales empleados (-o el sistema y la disponibilidad del líquido en forma pura. Los citados líquidos cubren una gama de -180 hasta 300 °C.
La presión de vapor aumenta con la temperatura más rápidamente a medida que la temperatura se eleva, de suerte que la curva temperatura presión de vapor no es lineal, y las gráficas de temperatura tienen sus marcas de grados mucho más separadas en el extremo superior de la escala que en el inferior. Un aparato registrador de 10 a 100 °C. puede tener divisiones de 2 grados C. entre 10 y 40 °C. y solamente de medio grado desde 40 hasta 100 °C. La exactitud de la lectura es escasa en el extremo inferior de la escala. La reproducibilidad de los termómetros de vapor a presión es del orden de +- 1 %, y en algunos casos considerablemente mejor.
El nivel del bulbo con respecto al aparato de medición de la presión es importante, pues si la temperatura del tubo de conexión es inferior a la temperatura del bulbo, el vapor se condensará en el tubo de conexión. El aparato de medición de la presión está sometido a la presión del vapor en el bulbo más la carga hidrostática de esta columna de líquido si el bulbo está sobre el aparato de medición, o a la presión del vapor en el bulbo menos la carga hidrostática si el bulbo está bajo el aparato de medida. Si la temperatura de operación del bulbo ha de ser más alta que la temperatura del aparato de medida de la presión, el instrumento se gradúa para una diferencia de nivel definida, Deben hacerse correcciones si se cambia la elevación del bulbo.
Un gran defecto en este sistema de medida es el trastorno debido al paso del líquido desde el bulbo al elemento de presión, o inversarnente, cuando la temperatura medida cruza la temperatura del instrumento.
Termómetros de líquido en dilatación
En un termómetro de líquido en dilatación, el sistema se llena completamente con un líquido apropiado y consiste en un bulbo conectado por tubo capilar a un elemento en forma de hélice o espiral de Bourdon situado en la caja del instrumento. A medida que aumenta la temperatura y se dilata el líquido, la hélice tiende a deshacerse para proporcionar el aumento de volumen y es mayor. La presión de llenado elegida debe ser tal, que la temperatura de ebullición del líquido sea apreciablemente más alta que la mayor temperatura que el sistema haya de medir. Pueden medirse temperaturas desde -1 75 °C. hasta + 300 °C. (550 °C. para el mercurio). Aunque los cambios de volumen son relativamente pequeiios, las fuerzas ejercidas pueden ser grandes para
accionar el elemento, y por consiguiente, este tipo de medida se considera bueno para aparatos reguladores que requieran alto grado de estabilidad.
El origen mayor de error en este tipo de medida es la dilatación térinica del líquido que no está en el bulbo. Cuando la longitud del tubo es corta, el error está en su mayor parte en el elemento Bourdon, y normalmente se coloca un elemento bimetálico de corrección en la caja para compensar este error.
Cuando el tubo capilar es largo, se usa uno de estos dos métodos para la corrección:
- 1) Un hilo metálico central se coloca en el tubo capilar en toda su longitud; este hilo tiene un coeficiente de dilatación que corrige el cambio de volumen de] líquido. Normalmente se emplea esto únicamente en los sistemas llenos con mercurio.
- 2) Un segundo tubo capilar sin bulbo, cerrado en el extremo correspondiente al bulbo, va paralelo al tubo capilar desde el bulbo y acciona un Bourdon helicoidal idéntico en la caja del instrumento, de tal modo enlazado con el elemento original, que cualquier dilatación en este capilar corrector se resta del otro sistema y corrige toda dilatación, excepto la del bulbo medidor.
Cualquier dilatación térmica del bulbo es incluida automáticamente en la graduación del sistema. La dilatación térmica del tubo capilar y del elemento sensible, son del todo insignificantes.


 =
= ![1 \left [ \frac{cal}{gC} \right ]](http://upload.wikimedia.org/math/d/5/a/d5aed3d8d24445d83da6d3f8a081430f.png)
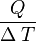
![\left [ \frac{J}{K} \right ]](http://upload.wikimedia.org/math/2/8/a/28a965e43a814809c9426baece39a88c.png)
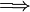 C = mc
C = mc